Химия 11 класс (Урок№8 - Химические источники тока. Ряд стандартных электродных потенциалов.)
Химия 11 класс
Урок№8 - Химические источники тока. Ряд стандартных электродных потенциалов.
мы узнаем:
как устроен гальванический элемент;
какие химические процессы в нем протекают;
мы научимся:
собирать схему гальванического элемента;
использовать возможности ряда напряжений металлов;
мы сможем:
составлять уравнения реакций, протекающих на электродах;
решать типовые задачи.
Гальванический элемент, аккумулятор, топливный элемент – устройства, в которых химическая энергия превращается в электрическую. Процессы окисления и восстановления в них разделены. Направленное движение электронов по проводнику от анода к катоду представляет собой электрический ток.
В аккумуляторе превращение химической энергии в электрическую происходит многократно.
В топливном элементе окислитель и восстановитель хранятся вне устройства и подаются к электродам во время работы.
Путём сравнения металлических электродов со стандартным водородным можно установить электродные потенциалы металлов. Расположив их в порядке возрастания, мы получим ряд стандартных водородных потенциалов.
Аккумулятор – химический источник тока многоразового действия.
Анод – электрод, на котором происходит процесс окисления. В электрохимии это часть электрохимической системы, включающая в себя проводник и окружающий его раствор.
Гальванический элемент – химический источник электрического тока, основанный на взаимодействии двух металлов и/или их оксидов в электролите, приводящем к возникновению в замкнутой цепи электрического тока.
Катод – электрод, на котором происходит процесс восстановления.
Ряд стандартных электродных потенциалов – ряд металлов, расположенных в порядке возрастания значения их стандартных потенциалов.
Стандартные условия – температура 25 оC, концентрация солей 1 моль/л, давление 0,1 МПа.
Стандартный водородный электрод – электрод, использующийся в качестве электрода сравнения при различных электрохимических измерениях.
Топливный элемент – устройство, обеспечивающее прямое преобразования химической энергии в электрическую.
Электрод – электрический проводник, имеющий электронную проводимость и находящийся в контакте с ионным проводником – электролитом.
Электрохимия – наука, которая изучает закономерности взаимного превращения химической и электрической форм энергии.
Видео Химия 11 класс (Урок№8 - Химические источники тока. Ряд стандартных электродных потенциалов.) канала LiameloN School
Урок№8 - Химические источники тока. Ряд стандартных электродных потенциалов.
мы узнаем:
как устроен гальванический элемент;
какие химические процессы в нем протекают;
мы научимся:
собирать схему гальванического элемента;
использовать возможности ряда напряжений металлов;
мы сможем:
составлять уравнения реакций, протекающих на электродах;
решать типовые задачи.
Гальванический элемент, аккумулятор, топливный элемент – устройства, в которых химическая энергия превращается в электрическую. Процессы окисления и восстановления в них разделены. Направленное движение электронов по проводнику от анода к катоду представляет собой электрический ток.
В аккумуляторе превращение химической энергии в электрическую происходит многократно.
В топливном элементе окислитель и восстановитель хранятся вне устройства и подаются к электродам во время работы.
Путём сравнения металлических электродов со стандартным водородным можно установить электродные потенциалы металлов. Расположив их в порядке возрастания, мы получим ряд стандартных водородных потенциалов.
Аккумулятор – химический источник тока многоразового действия.
Анод – электрод, на котором происходит процесс окисления. В электрохимии это часть электрохимической системы, включающая в себя проводник и окружающий его раствор.
Гальванический элемент – химический источник электрического тока, основанный на взаимодействии двух металлов и/или их оксидов в электролите, приводящем к возникновению в замкнутой цепи электрического тока.
Катод – электрод, на котором происходит процесс восстановления.
Ряд стандартных электродных потенциалов – ряд металлов, расположенных в порядке возрастания значения их стандартных потенциалов.
Стандартные условия – температура 25 оC, концентрация солей 1 моль/л, давление 0,1 МПа.
Стандартный водородный электрод – электрод, использующийся в качестве электрода сравнения при различных электрохимических измерениях.
Топливный элемент – устройство, обеспечивающее прямое преобразования химической энергии в электрическую.
Электрод – электрический проводник, имеющий электронную проводимость и находящийся в контакте с ионным проводником – электролитом.
Электрохимия – наука, которая изучает закономерности взаимного превращения химической и электрической форм энергии.
Видео Химия 11 класс (Урок№8 - Химические источники тока. Ряд стандартных электродных потенциалов.) канала LiameloN School
Показать
Комментарии отсутствуют
Информация о видео
Другие видео канала
 Основы электрохимии
Основы электрохимии Продукты в ОВР. Ч.2-1. Электродный потенциал металлов.
Продукты в ОВР. Ч.2-1. Электродный потенциал металлов. Химические источники тока. Урок №2
Химические источники тока. Урок №2 Урок 143 (осн). Электрический ток. Источники тока
Урок 143 (осн). Электрический ток. Источники тока Химия 11 класс (Урок№6 - Дисперсные системы.)
Химия 11 класс (Урок№6 - Дисперсные системы.) 12. Разновидности источников тока
12. Разновидности источников тока Химия 11 класс (Урок№9 - Коррозия металлов и её предупреждение.)
Химия 11 класс (Урок№9 - Коррозия металлов и её предупреждение.) Ряд стандартных электродных потенциалов металлов или электрохимический ряд напряжений. Урок #23
Ряд стандартных электродных потенциалов металлов или электрохимический ряд напряжений. Урок #23 Что такое старение?
Что такое старение? Постоянный электрический ток. Источники электрического тока. 8 класс.
Постоянный электрический ток. Источники электрического тока. 8 класс.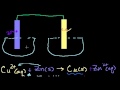 Гальванические элементы
Гальванические элементы ОВР: как решать быстро и правильно | ХИМИЯ ЕГЭ | Лия Менделеева
ОВР: как решать быстро и правильно | ХИМИЯ ЕГЭ | Лия Менделеева Химия аккумуляторов — Даниил Иткис / ПостНаука
Химия аккумуляторов — Даниил Иткис / ПостНаука
 Дисперсные системы | Химия 11 класс #11 | Инфоурок
Дисперсные системы | Химия 11 класс #11 | Инфоурок 10.2. Альдегиды и кетоны: Способы получения. ЕГЭ по химии
10.2. Альдегиды и кетоны: Способы получения. ЕГЭ по химии Генератор
Генератор 6. Химические источники тока. Гальванический элемент
6. Химические источники тока. Гальванический элемент ЭКЗО- и ЭНДО- термические реакции. Химия – Просто
ЭКЗО- и ЭНДО- термические реакции. Химия – Просто Химия 47. Химический источник тока. Электролиз — Академия занимательных наук
Химия 47. Химический источник тока. Электролиз — Академия занимательных наук