Химия 11 класс (Урок№3 - Пространственное строение молекул.)
Химия 11 класс
Урок№3 - Пространственное строение молекул.
мы узнаем:
о типах гибридизации атомных орбиталей;
мы научимся:
объяснять пространственное строение молекул органических и неорганических соединений с помощью представлений о гибридизации орбиталей;
мы сможем:
решать типовые задачи.
Гибридизацией называют образование одинаковых по энергии и форме орбиталей атома в результате сложения различных по энергии и форме орбиталей при возбуждении этого атома. При этом орбитали разной симметрии смешиваются и переходят в гибридные атомные орбитали одинаковой формы и одинаковой усредненной энергии, что обеспечивает равноценность образуемых ими связей. Различают sp, sp2,sp3 –гибридизацию.
Типы связи
Существует несколько типов связи. Связь, образованная перекрыванием атомных орбиталей по линии, соединяющей ядра взаимодействующих атомов, называется σ-связью. Сигма-связь может возникать при перекрывании s-орбиталей, s и р-орбиталей, d-орбиталей, а также d и s-орбиталей, d и p-орбиталей и f-орбиталей друг с другом и другими орбиталями. Сигма-связь обычно охватывает два атома и не простирается за их пределы, поэтому является локализованной двухцентровой связью. Она имеет осевую симметрию, и оба атома могут вращаться вдоль линии связи, т.е. той воображаемой линии, которая проходит через ядра химически связанных атомов. Это исключает возможность образования пространственных изомеров.
Связь, образованная перекрыванием атомных орбиталей по обе стороны линии, соединяющей ядра атомов (боковые перекрывания), называется π-связью. π-связь может образовываться при перекрывании р и р-орбиталей, р и d-орбиталей, d и d-орбиталей, а также f и p- , f и f-орбиталей.
Связь, образованная перекрыванием d-орбиталей всеми четырьмя лепестками, называется δ-связью (дельта-связь). Соответственно s-элементы могут образовывать только σ-связи; р-элементы – σ и p-связи, d-элементы – δ, p и σ-связи, а f-элементы – δ-, p-, σ- и еще более сложные связи. В связи с меньшим перекрыванием атомных орбиталей прочность у π- и δ-связей ниже, чем у σ-связей.
При наложении π-связи на σ-связь образуется двойная связь, например в молекулах кислорода (О = О), этилена (СН2 = СН2), диоксида углерода (O = С = O). Хотя энергия π-связи меньше, чем энергия σ–связи, однако суммарная энергия двойной связи выше энергии одинарной связи, а длина двойной связи меньше длины одинарной связи.
При наложении двух π-связей на σ-связь возникает тройная связь, например в молекулах азота (N ≡ N) и ацетилена (СН ≡ СН). Энергия тройной связи выше, а длина связи меньше, чем энергии и длины простой и двойной связей. Число связей между атомами называется кратностью связи. Каждая кратная связь всегда содержит только одну σ-связь. Число σ-связей, которые образует центральный атом в сложных молекулах или ионах, определяет для него значение координационного числа. Например, в молекуле NH3 и ионе NH4+ для атома азота оно равно трем и четырем соответственно.
Видео Химия 11 класс (Урок№3 - Пространственное строение молекул.) канала LiameloN School
Урок№3 - Пространственное строение молекул.
мы узнаем:
о типах гибридизации атомных орбиталей;
мы научимся:
объяснять пространственное строение молекул органических и неорганических соединений с помощью представлений о гибридизации орбиталей;
мы сможем:
решать типовые задачи.
Гибридизацией называют образование одинаковых по энергии и форме орбиталей атома в результате сложения различных по энергии и форме орбиталей при возбуждении этого атома. При этом орбитали разной симметрии смешиваются и переходят в гибридные атомные орбитали одинаковой формы и одинаковой усредненной энергии, что обеспечивает равноценность образуемых ими связей. Различают sp, sp2,sp3 –гибридизацию.
Типы связи
Существует несколько типов связи. Связь, образованная перекрыванием атомных орбиталей по линии, соединяющей ядра взаимодействующих атомов, называется σ-связью. Сигма-связь может возникать при перекрывании s-орбиталей, s и р-орбиталей, d-орбиталей, а также d и s-орбиталей, d и p-орбиталей и f-орбиталей друг с другом и другими орбиталями. Сигма-связь обычно охватывает два атома и не простирается за их пределы, поэтому является локализованной двухцентровой связью. Она имеет осевую симметрию, и оба атома могут вращаться вдоль линии связи, т.е. той воображаемой линии, которая проходит через ядра химически связанных атомов. Это исключает возможность образования пространственных изомеров.
Связь, образованная перекрыванием атомных орбиталей по обе стороны линии, соединяющей ядра атомов (боковые перекрывания), называется π-связью. π-связь может образовываться при перекрывании р и р-орбиталей, р и d-орбиталей, d и d-орбиталей, а также f и p- , f и f-орбиталей.
Связь, образованная перекрыванием d-орбиталей всеми четырьмя лепестками, называется δ-связью (дельта-связь). Соответственно s-элементы могут образовывать только σ-связи; р-элементы – σ и p-связи, d-элементы – δ, p и σ-связи, а f-элементы – δ-, p-, σ- и еще более сложные связи. В связи с меньшим перекрыванием атомных орбиталей прочность у π- и δ-связей ниже, чем у σ-связей.
При наложении π-связи на σ-связь образуется двойная связь, например в молекулах кислорода (О = О), этилена (СН2 = СН2), диоксида углерода (O = С = O). Хотя энергия π-связи меньше, чем энергия σ–связи, однако суммарная энергия двойной связи выше энергии одинарной связи, а длина двойной связи меньше длины одинарной связи.
При наложении двух π-связей на σ-связь возникает тройная связь, например в молекулах азота (N ≡ N) и ацетилена (СН ≡ СН). Энергия тройной связи выше, а длина связи меньше, чем энергии и длины простой и двойной связей. Число связей между атомами называется кратностью связи. Каждая кратная связь всегда содержит только одну σ-связь. Число σ-связей, которые образует центральный атом в сложных молекулах или ионах, определяет для него значение координационного числа. Например, в молекуле NH3 и ионе NH4+ для атома азота оно равно трем и четырем соответственно.
Видео Химия 11 класс (Урок№3 - Пространственное строение молекул.) канала LiameloN School
Показать
Комментарии отсутствуют
Информация о видео
Другие видео канала
 Гибридизация - смысл. Разбор 10 молекул:CH4, NH3, H2O, C2H4, BCl3, SO2, SO3, BeCl2, CO2, C2H2.
Гибридизация - смысл. Разбор 10 молекул:CH4, NH3, H2O, C2H4, BCl3, SO2, SO3, BeCl2, CO2, C2H2. Гибридизация. Полярные и неполярные молекулы. Самоподготовка к ЕГЭ и ЦТ по химии
Гибридизация. Полярные и неполярные молекулы. Самоподготовка к ЕГЭ и ЦТ по химии Гибридизация атомных орбиталей и геометрия молекул. 10 класс.
Гибридизация атомных орбиталей и геометрия молекул. 10 класс.
 Химия 11 класс (Урок№1 - Хим. элемент. Нуклиды. Изотопы. Законы сохранения массы и энергии в химии.)
Химия 11 класс (Урок№1 - Хим. элемент. Нуклиды. Изотопы. Законы сохранения массы и энергии в химии.) Трёхмерные схематические структурные формулы (видео 23) | Химические связи и структура молекул
Трёхмерные схематические структурные формулы (видео 23) | Химические связи и структура молекул Модели строения атома
Модели строения атома Химия 11 класс (Урок№4 - Строение кристаллов. Кристаллические решётки.Причины многообразия веществ.)
Химия 11 класс (Урок№4 - Строение кристаллов. Кристаллические решётки.Причины многообразия веществ.) Пи-связи и sp2-гибридизованные орбитали (видео 14) | Химические связи и структура молекул | Химия
Пи-связи и sp2-гибридизованные орбитали (видео 14) | Химические связи и структура молекул | Химия Зык Н. В. - Биоорганическая химия II - Углеводы. Моносахариды
Зык Н. В. - Биоорганическая химия II - Углеводы. Моносахариды Скорость химической реакции. Практическая часть. 10 класс.
Скорость химической реакции. Практическая часть. 10 класс. Система R,S определения абсолютной конфигурации
Система R,S определения абсолютной конфигурации Химия 11 класс (Урок№6 - Дисперсные системы.)
Химия 11 класс (Урок№6 - Дисперсные системы.) Химия 11 класс (Урок№13 - Сплавы металлов.)
Химия 11 класс (Урок№13 - Сплавы металлов.) Сигма- и пи-связи
Сигма- и пи-связи 14. Строение веществ (простых и сложных)
14. Строение веществ (простых и сложных) Комплексные соединения. 1 часть. 11 класс.
Комплексные соединения. 1 часть. 11 класс. 8 класс. Распределение электронов в атоме. Электронные формулы.
8 класс. Распределение электронов в атоме. Электронные формулы.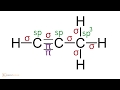 Гибридизация. Виды гибридизации. Теория для задания 12 ЕГЭ по химии.
Гибридизация. Виды гибридизации. Теория для задания 12 ЕГЭ по химии. 5. Строение вещества. Атомы и молекулы (часть 1)
5. Строение вещества. Атомы и молекулы (часть 1)