- Популярные видео
- Авто
- Видео-блоги
- ДТП, аварии
- Для маленьких
- Еда, напитки
- Животные
- Закон и право
- Знаменитости
- Игры
- Искусство
- Комедии
- Красота, мода
- Кулинария, рецепты
- Люди
- Мото
- Музыка
- Мультфильмы
- Наука, технологии
- Новости
- Образование
- Политика
- Праздники
- Приколы
- Природа
- Происшествия
- Путешествия
- Развлечения
- Ржач
- Семья
- Сериалы
- Спорт
- Стиль жизни
- ТВ передачи
- Танцы
- Технологии
- Товары
- Ужасы
- Фильмы
- Шоу-бизнес
- Юмор
The entropy change associated with the conversion of 1 kg of ice at 273 K to water vapours at 383 K
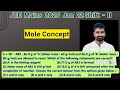
The entropy change associated with the conversion of 1 kg of ice at 273 K to water vapours at 383 K is (Specific heat of water liquid and water vapour are 4.2 kJ K K–1 kg–1 and 2.0 kJ K–1 kg–1 ; heat of liquid fusion and vapourisation of water are 344 kJ kg–1 and 2491 kJ kg–1, respectively). (log 273 = 2.436, log 373 = 2.572, log 383 = 2.583)
(1) 7.90 kJ K–1 kg–1
(2) 2.64 kJ K–1 kg–1
(3) 8.49 kJ K–1 kg–1
(4) 9.26 kJ K–1 kg–1
JEE Mains 2019 Jan 9 Shift - 2
#chemwarriors
#chemistrychamps
#solutionsmaster
#solutionpyqs
#solutionpyqs2019
#jeemains2025pyq
#pyqanalysis
#thermodynamicchemistryclass11
#thermodynamique
#thermodynamicschemistry
#thermodynamicsvideos
#neetpyqsolution2025
#jeepyqsolution
Видео The entropy change associated with the conversion of 1 kg of ice at 273 K to water vapours at 383 K канала Chem Warriors
(1) 7.90 kJ K–1 kg–1
(2) 2.64 kJ K–1 kg–1
(3) 8.49 kJ K–1 kg–1
(4) 9.26 kJ K–1 kg–1
JEE Mains 2019 Jan 9 Shift - 2
#chemwarriors
#chemistrychamps
#solutionsmaster
#solutionpyqs
#solutionpyqs2019
#jeemains2025pyq
#pyqanalysis
#thermodynamicchemistryclass11
#thermodynamique
#thermodynamicschemistry
#thermodynamicsvideos
#neetpyqsolution2025
#jeepyqsolution
Видео The entropy change associated with the conversion of 1 kg of ice at 273 K to water vapours at 383 K канала Chem Warriors
Комментарии отсутствуют
Информация о видео
20 ноября 2025 г. 20:31:26
00:12:21
Другие видео канала












![The calculated spin-only magnetic moments of K3[Fe(OH)6] and K4[Fe(OH)6] respectively are :#JEE](https://i.ytimg.com/vi/KAiPCjZkZsw/default.jpg)